Il trasporto inverso del colesterolo
Oggi facciamo un po’ di biologia molecolare più approfondita e parliamo di trasporto inverso del colesterolo (RCT: reverse cholesterol transport).
Questo articolo ci sarà utile per approfondire nei successivi articoli del blog di Cholenor aspetti fondamentali e di grande attualità come il collegamento tra colesterolo alto e tumori e tra colesterolo alto e infezioni virali come quella da SARS-CoV-2.
Ma facciamo uno step alla volta e iniziamo la nostra lezione!
Come tutte le cellule non intestinali od epatiche, le cellule periferiche non sono in grado di degradare il colesterolo in eccesso. Il trasporto inverso del colesterolo è il meccanismo fondamentale per mantenere l’omeostasi del colesterolo, finalizzato al recupero epatico del colesterolo periferico attraverso la sua incorporazione nelle lipoproteine HDL ed il successivo trasporto al fegato per l’escrezione biliare.
Perché il trasporto inverso del colesterolo è importante?
Quando il colesterolo si accumula in eccesso all’interno delle cellule diviene citotossico.
Quali sono le tappe che caratterizzano il trasporto inverso del colesterolo?
La biosintesi delle lipoproteine HDL passa attraverso la sintesi e la secrezione iniziale delle principali componenti proteiche (apoproteine), cui segue l’acquisizione extracellulare di lipidi (fosfolipidi e colesterolo) che porta all’assemblaggio ed alla generazione di particelle mature HDL.
La prima tappa del trasporto inverso del colesterolo consiste nella produzione, da parte dell’intestino e del fegato, di precursori discoidali delle HDL, che espongono sulla loro superficie apoproteine (principalmente ApoA-I).
Vengono così rilasciate molecole precorritrici delle HDL chiamate pre-B-HDL, che incorporano quantità piccolissime di colesterolo e lipidi, soprattutto fosfolipidi attraverso l’intervento di un trasportatore di membrana chiamato ATP-binding cassette A1 (ABCA1).
Questo trasportatore è localizzato sulla superficie cellulare e nelle membrane del Golgi, e può trasportare i lipidi dall’apparato di Golgi alla membrana cellulare, facilitandone poi l’efflusso.
A questo punto, non appena il colesterolo libero entra nelle HDL native, interviene un enzima plasmatico di origine epatica, chiamato plasma lecitin-colesterolo aciltrasferasi (LCAT), che converte il colesterolo libero incorporato nelle pre-B-HDL in esteri del colesterolo, trasformando, quindi, le molecole di pre-B-HDL nella loro forma “matura” α-HDL matura. Il processo di esterificazione mediato da LCAT è fondamentale per impedire la re-diffusione del colesterolo dalle HDL alla membrana plasmatica e permettere alle HDL di continuare ad acquisire apoproteine dalle particelle lipoproteiche ricche in trigliceridi e fondersi tra loro.
Nell’intero processo, l’apolipoproteina AI svolge un ruolo chiave, stimolando sia l’attività del trasportatore ABCA1 che quella della LCAT. Poiché l’ApoAI è l’apolipoproteina maggiormente rappresentata nelle HDL, la sua concentrazione plasmatica risulta direttamente correlata ai livelli di colesterolo HDL.
Queste lipoproteine vengono trasportate, quindi, al fegato, dove rilasciano il colesterolo, secondo due vie distinte.
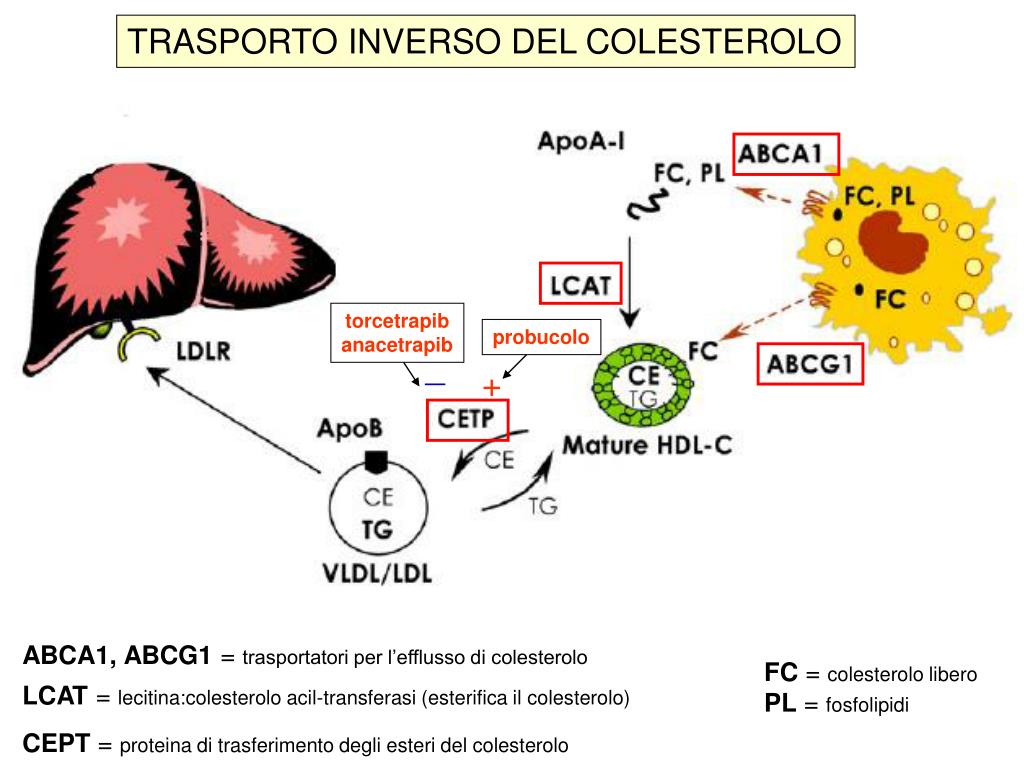
Prima via epatica
In un primo caso, le HDL ricche in colesterolo esterificato cedono questo lipide alle lipoproteine ricche in trigliceridi (lipoproteine a bassissima e a bassa densità), poi intercettate dal fegato mediante specifici recettori (LDL-R) e rimosse dalla circolazione.
Lo scopo è quello di veicolare il colesterolo periferico al fegato tramite il sistema dell’LDL recettore, quindi “scaricare” a livello periferico le HDL dall’eccesso di colesterolo, in modo da renderle nuovamente disponibili ad accoglierlo dai tessuti. Svuotandosi di colesterolo, le HDL accettano in cambio trigliceridi e ciò avviene grazie alla proteina di trasferimento degli esteri del colesterolo (CETP).
Seconda via epatica
La seconda via coinvolge recettori epatici SR-B1 per le HDL ricche in colesterolo esterificato, in assenza di concomitante degradazione della porzione proteica delle HDL, che viene quindi riciclata. In pratica, quest’enzima consente di svuotare le HDL dal loro contenuto e rigenerare nuove pre-B-HDL.
Parte delle HDL e delle ApoA-I viene anche internalizzata e degradata a livello lisosomiale, sia nelle cellule epatiche che in quelle renali.



